管式反应炉制取二硫化碳反应的研究
Outline:
娄少华

,
钱永康
收稿日期:2010-09-13;修回日期:2010-09-25
作者简介:
娄少华:汉族,1984年出生,北京航天动力研究所硕士研究生。联系方式:15001221910,邮箱:
loushh@calt11.cn,地址:(100076)北京市丰台区南大红门路一号运载火箭技术研究院,9200信箱11分箱.
摘要:本文依据甲烷与硫磺反应生成二硫化碳的相关数据,由化学反应动力学理论计算出硫磺分解的动力学数据,得到包括6个主要反应机理的计算模型。利用计算流体力学软件FLUENT对生成二硫化碳的反应进行模拟计算,寻找影响二硫化碳产率的因素,从而对管式反应器的设计和优化等提供理论依据。
关键词:二硫化碳 反应机理 管式反应炉 优化
Study on Carbon Disulfide Reaction in Tubular Reacting Furnace
Outline:
Lou Shaohua

,
Qian Yongkang
Beijing Aerospace Propulsion Institute
Abstract: In the paper, six main reactions are summarized to form the mathematics model, according to the correlative data analysis of methane reacting with sulfur and sulfur molecule decomposition. The reaction process was simulated and calculated with Fluent hydrodynamic software and the influential factors on carbon disulfide productive rate would be found out, the reaction process is simulated by the hydrodynamic software of Fluent, which will provide theoretical basis for design and optimization of tubular reacting furnace.
Key words:
carbon disulfide reaction mechanism tubular reacting furnace optimization
二硫化碳有广泛用途,比如用于粘胶纤维、玻璃纸、溶剂,橡胶促进剂等,工业上广泛采用甲烷法制取。本文针对液体硫磺与甲烷反应进行分析,应用CFD方法模拟管内的反应过程,得出温度、压力等因素的影响规律,对反应过程优化提供理论依据。
1 国内外发展现状
用甲烷法制取二硫化碳的反应是由Carlisle M.Thacker发现的,他致力于研究用液体汽油的馏分来制取二硫化碳,Shawinigan研究基于Fluohmic加热炉用硫磺或者硫化氢作为反应物的方法。目前,国外普遍采用的甲烷法有:改良FMC、Stauffer和PPG技术,国外装置规模和生产能力很大,国内外还存在较大差距。
2 反应过程的研究
本文针对改良FMC工艺,即甲烷与硫磺非催化反应,分析其中的硫磺的汽化和硫磺与甲烷的反应两部分。
2.1 硫磺汽化过程
在温度较低时硫磺的分子是由8个硫原子组成的,呈环状排列。当加热时粘度逐渐升高,继续加热到200 ℃,粘度开始下降,当温度达到444.45 ℃时,液体硫磺开始变成蒸汽,蒸汽中有S8、S6、S4、S2等分子存在,随着温度的升高,含原子数少的分子占的比重增大。继续加热到1 200 ℃以上时,硫蒸汽离解成硫原子。
2.2 反应机理的分析
分析研究[1]发现, 在500 ℃~800 ℃时甲烷与硫磺都能发生反应,当温度小于1 100 ℃时,主要生成H2S、CS2,而当温度高于1 100 ℃时,就会有明显的副反应发生,并且生成CS2的反应是二级。同时还发现硫磺的分解反应是快速反应,生成CS2的反应是总反应体系的控制步[2]。本文根据文献[3, 4]中的实验数据,整理得相关反应动力学数据,见表 1。
表 1

|
表 1 反应机理
|
对硫分子的分解反应主要是(4)、(5)两个反应,动力学数据根据连续性反应和分子碰撞理论[5, 6],以及计算的数据与实测数据的对比修改而得到。
2.3 结焦过程分析
天然气法生产过程中烃裂解析碳结焦是不可避免的,温度较低时,烷烃裂解生成分子量小的烷烃和烯烃。裂解产生的烷烃在高温下裂解生成更小的分子,进一步发生脱氢反应。环烷烃热稳定性较高,主要发生脱氢反应生成芳烃,最后生成油状物[4]。烃类裂解的最终重质产物是炭和焦油,加之硫磺中的机械杂质和设备管路的腐蚀产物掺合在一起形成固态物质。因结焦过程复杂,为了简化计算过程,主要研究生成CS2的反应,结焦过程用反应(6)来表示。
3 反应过程的数值模拟
把上述的反应机理通过CFD模拟计算与实际数据进行对比,通过模拟计算就可以得到不同的因素对产物的收率的影响。
3.1 数学模型
管式反应器的数学模型由质量、动量、能量、组分等守恒方程组及湍流双方程、两相流和反应动力学模型构成。计算过程借助于流体力学软件FLUENT对上述数学模型进行求解,采用二阶迎风格式及Simple算法耦合求解[7]。
对于蒸发过程的处理:通过编程计算出444.45 ℃时气态硫磺各组分的分布,作为初始液体硫磺的组成,在蒸发过程中忽略分解反应。蒸发过程用Lee提出的蒸发理论模型[8],把蒸发过程质量与能量方程的源项用UDF定义,其中硫的汽化潜热为9.358 kJ/mol[9]。计算中使用mixture模型,用下标p表示汽相,q表示液相,局部温度T≥Tsat时,质量源项与局部温度有如下的关系:
 |
(1) |
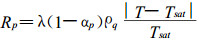 |
(2) |
3.2 计算区域网格
模拟计算的管式反应器,是由26根长度是6.1 m的水平管连接成的蛇形管。物料从水平反应管的上部进入, 依次经过气体预热段、蒸发段和反应段,本文重点计算了蒸发段和反应段。蒸发段主要是液体蒸发,反应段主要进行反应,对称的计算区域网格划分如图 1所示。
3.3 边界条件
根据相关的测量数据整理出管壁温度边界,由编程计算出硫磺三种组分S2、S6、S8的分布作为入口处的质量边界。
3.3.1 温度边界
根据工业测量的管壁面温度拟合得出管壁面的温度,蒸发段主要是液体蒸发,化学反应作用可以忽略,反应段前部主要是硫磺分子的分解反应,需要较高的温度。因此,入口处的温度应该较高,有利于反应的进行。随着生成二硫化碳的反应开始增加,吸热量会有下降。
3.3.2 入口边界
由热力学参数计算出平衡常数[6],进而计算出不同条件下硫磺的三种组分的分布,如图 2所示。
与朱利凯等[10]得出的不同压力和温度下的S2、S6和S8分布对比发现,计算的结果误差小于5%。设置操作压力是1.1 MPa,入口物料的温度是490 K,甲烷、氮气质量流量分别为0.087 311 kg/s、0.001 05 kg/s。相关物料的热传导率、粘度的拟合数据[11],拟合多项式如下:
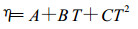 |
(3) |
 |
(4) |
4 CFD计算分析
在FLUENT中设置相应的数学模型和初始条件,对于管内的反应和蒸发过程进行计算,分析计算结果,对管式反应器提出优化改进措施。
4.1 蒸发过程
气相体积分数云图,如图 3所示。由图 3可以看出,在1~4号管内基本完成蒸发过程,温度越低的混合物越靠近下部,越靠近壁面处,混合物的温度越高,气体体积分数就越大,同时在蒸发段内管径方向存在较大的温度梯度。
4.2 组分沿管长度方向分布
通过模拟计算管内物料的温度、速度、组分和云图,如图 4~图 9所示。在温度升高到717 K时,硫磺液体开始蒸发,同时CH4的体积分数开始下降,这时硫磺蒸汽中主要是S8、S6,而S2的量很少;在随后的流动过程中,硫磺开始分解;CS2的浓度逐渐增加至30%左右,但是在最后3根管内CS2的摩尔分数变化不大;随着温度的升高,CH4裂解反应会有明显的增加。
计算结果和工业测量数据对比,见表 2。由表 2可以看出,FLUENT计算与实际符合较好,上述的反应机理能够较好地描述反应管内的反应过程。
表 2

|
表 2 计算结果与工业测量数据对比
|
4.3 反应管的换热量
在反应管前部进行硫磺分解反应,介质要吸收大量的热量,后部主要进行CS2的放热反应,介质吸收的热量有所减少。在反应段内吸热率的误差较大,因为根据实测的温度计算的传热率是不精确的。如表 3所示。
表 3

|
表 3 传热率对比
|
5 管式反应器的优化
5.1 温度变化规律
在温度大于1 050 K时,总反应的热效应为放热,提高温度对提高转化率不利;温度低时,提高温度对提高平衡转化率是有利的,因此,可以为反应选择适当高的温度来提高反应速率。但当温度过高时,硫磺蒸汽的腐蚀性加剧,所以反应温度应控制在1 000 K左右。
5.2 管子结构
从计算结果可以看出,现在模型中用到的反应管长度可以减少12 m。另外,增加反应管的直径,在管内径上,温度梯度变大,反应管要承受更大的热应力作用,烃类热裂解的速率也会加快,更容易形成结焦层。
5.3 入口组分的比例
甲烷过量时其转化率会降低,硫磺的转化率会提高,但是甲烷裂解反应会在反应管内产生结焦;高碳烃更易发生裂解,应该减少原料气中高碳烃的比例。适当增加硫磺比例,过量的部分可以通过冷凝回收循环使用。在天然气含重烃的量不多时,硫磺一般可以选择过量5%~10%。
6 结论
通过分析总结得出了符合CS2管式反应炉的反应机理,为优化CS2管式反应器设计提供了理论依据。本文需要改进之处:进行理论推导得出更加详细的反应机理;把管内反应与炉膛内的燃烧过程耦合在一起计算。
| [1] |
|
| [2] |
|
| [3] |
Fisher R A and Smith J M. Kinetics of reaction between methane and sulfur vapor[J]. Industrial and Engineering Chemistry, 1950, 42(4): 704-709. DOI:10.1021/ie50484a039 |
| [4] |
|
| [5] |
许越. 化学反应动力学[M]. 北京: 化学工业出版社, 2005: 43.
|
| [6] |
范康年. 物理化学[M]. 第二版.北京: 高等教育出版社, 2005: 350.
|
| [7] |
王福军. 计算流体力学动力学分析-CFD软件原理与应用[M]. 北京: 清华大学出版社, 2004: 74.
|
| [8] |
Brian St. Rock.Thermal-fluid analysis of a lithium vaporizer for a high power magnetoplasmadnamic thruster, June, 2006.
|
| [9] |
Stull D R. Thermodynamics of carbon disulfide production[J]. Industrial and Engineering Chemistry, 1949, 41(9): 1968-1973. DOI:10.1021/ie50477a031 |
| [10] |
|
| [11] |
Carl L. Yaws.Chemical Properties handbook.McGraw-Hill Book Co, 1999: 16.
|
 2011, Vol. 40
2011, Vol. 40  Issue (1): 18-21
Issue (1): 18-21
 2011, Vol. 40
2011, Vol. 40  Issue (1): 18-21
Issue (1): 18-21